賓夕法尼亞大學(xué)佩雷爾曼醫(yī)學(xué)院的科學(xué)家進(jìn)行的一項(xiàng)新研究顯示����,在許多胰腺腫瘤的發(fā)展中經(jīng)常發(fā)生的DNA突變似乎使這些癌癥易受稱為PARP抑制劑的現(xiàn)有藥物的攻擊����。
該發(fā)現(xiàn)近日發(fā)表在了《科學(xué)進(jìn)展》上����。研究表明�����,在最常見的胰腺腫瘤類型中�����,多達(dá)三分之二的患者病例在腫瘤細(xì)胞中缺失了該基因的一個(gè)拷貝�����。賓夕法尼亞大學(xué)的科學(xué)家發(fā)現(xiàn)�����,盡管這種刪除似乎有助于腫瘤生長(zhǎng),但腫瘤細(xì)胞中MYBBP1A剩余拷貝的丟失卻具有相反的作用���,從而大大降低了細(xì)胞的生長(zhǎng)�����。

該小組通過在胰腺癌細(xì)胞和小鼠模型中進(jìn)行的實(shí)驗(yàn)證明���,他們可以利用稱為PARP1抑制劑的現(xiàn)有藥物中的某些成員來利用此漏洞,這種藥物可以在MYBBP1A蛋白的水平已經(jīng)很低時(shí)使其失活�����。目前�,PARP1抑制劑主要用于治療卵巢癌和乳腺癌。
細(xì)胞與發(fā)育學(xué)教授肯尼斯·扎雷特(Kenneth Zaret)博士表示����,某種類型的DNA缺失在胰腺癌中經(jīng)常發(fā)生,他們?cè)诩?xì)胞和動(dòng)物實(shí)驗(yàn)中發(fā)現(xiàn)�,這種DNA缺失使這些癌癥對(duì)已有藥物有選擇性的敏感性。這是一個(gè)令人振奮的發(fā)現(xiàn)�����,因?yàn)槟壳皼]有針對(duì)胰腺癌的高效治療方法;而且�,該方法原則上可以用于尋找其他具有DNA缺失特征的癌癥的新治療方法。
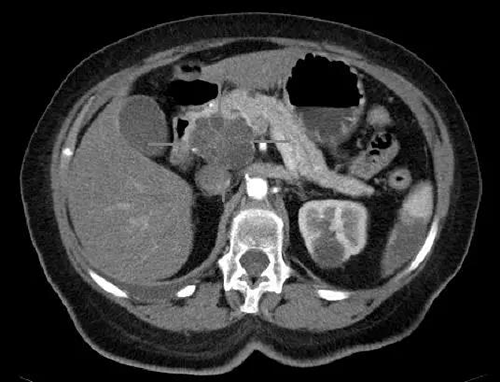
胰頭癌和囊腺癌具有iv對(duì)比度的軸向CT圖像(圖片來源:Science)
美國(guó)癌癥協(xié)會(huì)估計(jì)��,每年在美國(guó)有將近 60,000 人被診斷患有胰腺癌�����,其中近 50,000 人死于這些癌癥�。胰腺癌的治愈率非常低����,主要是因?yàn)檫@些癌癥往往僅在晚期開始在體內(nèi)擴(kuò)散時(shí)才被發(fā)現(xiàn),并且對(duì)化學(xué)療法和其他療法具有相對(duì)的抵抗力���,因此迫切需要更好的胰腺癌治療方法����。
胰腺癌�、胰管腺癌或 PDAC 是最常見的形式,通常具有部分刪除 17 號(hào)染色體的特征����。人類細(xì)胞具有 22 對(duì)染色體以及X和Y性染色體���。在 PDAC 中丟失了第 17 號(hào)染色體一個(gè)拷貝的一部分,意味著位于該染色體上的許多基因僅剩下一個(gè)拷貝�,因此這些基因編碼的蛋白質(zhì)水平降低了。這最終會(huì)促進(jìn)受影響的癌細(xì)胞的生長(zhǎng)����,部分原因是受影響的蛋白質(zhì)之一是腫瘤抑制物 P53,它通??勺鳛閺?qiáng)大的故障安全開關(guān),防止細(xì)胞過度分裂��。
Zaret實(shí)驗(yàn)室的美國(guó)胃腸病學(xué)博士后研究員 Antony Hsieh 博士在研究期間想知道�����,這些 17 號(hào)染色體缺失中其他基因的丟失是否會(huì)使 PDAC 細(xì)胞變得脆弱��,從而可以利用未來或現(xiàn)有的藥物進(jìn)行開發(fā)����。他最終選擇了 MYBBP1A。
Hsieh及其同事發(fā)現(xiàn)�,在缺失 17號(hào) 染色體的 PDAC 細(xì)胞中,MYBBP1A 的一個(gè)拷貝丟失��,使細(xì)胞更加癌變,從而增加了 P53 部分丟失的促生長(zhǎng)作用�����。另一方面�����,科學(xué)家發(fā)現(xiàn)��,使用基因工程技術(shù)使 MYBBP1A 的其余拷貝失活����,有效地阻滯了 PDAC 細(xì)胞癌性生長(zhǎng)的剎車。
通過回顧生物學(xué)文獻(xiàn)并進(jìn)行自己的實(shí)驗(yàn)��,科學(xué)家還發(fā)現(xiàn) MYBBP1A 蛋白作用于細(xì)胞核 DNA 上��,以促進(jìn)生長(zhǎng)基因的活性����,并與稱為 PARP1 蛋白的蛋白緊密相互作用�����。這暗示了治療的機(jī)會(huì),因?yàn)檠芯咳藛T最近開發(fā)了一種稱為 PARP1 抑制劑的抗癌藥物���。
PARP1 抑制劑被批準(zhǔn)用于治療乳腺癌和卵巢癌���,其作用機(jī)理與 MYBBP1A 無關(guān)。但是���,某些 PARP1 抑制劑似乎是通過將 PARP1 蛋白捕獲在細(xì)胞核中卷曲的 DNA上而部分起作用的����。正如 Penn Medicine 小組發(fā)現(xiàn)的那樣��,以這種方式捕獲PARP1 的 PARP1 抑制劑(即藥物 olaparib 和 niraparib)從染色體上排出了殘留量的 MYBBP1A 蛋白���,從而破壞了其在細(xì)胞核中的生長(zhǎng)促進(jìn)功能����。在具有兩個(gè) MYBBP1A 基因的工作拷貝和充足的 MYBBP1A 蛋白供應(yīng)的細(xì)胞中����,這些藥物似乎無效。但是在丟失了一份 MYBBP1A 拷貝的 PDAC 細(xì)胞中�����,這些藥物具有終止生長(zhǎng)的作用,例如完全敲除 MYBBP1A 基因�����。
該團(tuán)隊(duì)在使用 PDAC 細(xì)胞的實(shí)驗(yàn)皿實(shí)驗(yàn)中證明了這一點(diǎn)���,并表明�,在移植了缺少一個(gè)MYBBP1A 拷貝的人 PDAC 細(xì)胞的小鼠中�����,用 olaparib 治療小鼠的腫瘤要比未經(jīng)治療的未經(jīng)移植的小鼠小得多���。
結(jié)果表明����,奧拉帕尼和尼拉帕利布可能對(duì)成千上萬例胰腺腫瘤細(xì)胞僅含有一份MYBBP1A 的患者具有實(shí)質(zhì)性益處研究人員希望這些發(fā)現(xiàn)可以鼓勵(lì)其他人將癌癥中遺傳物質(zhì)的損失視為開發(fā)針對(duì)這些癌癥的新策略的機(jī)會(huì)��。
研究人員將通過進(jìn)一步的臨床前實(shí)驗(yàn)以及進(jìn)行 PARP1 抑制劑在選定的胰腺癌患者中的臨床試驗(yàn)����,以加快其 PARP1 抑制劑策略的開發(fā)。作為這項(xiàng)工作的一部分����,科學(xué)家們正在與醫(yī)學(xué)博士 Kojo Elenitoba-Johnson ,賓夕法尼亞大學(xué)醫(yī)學(xué)博士 Peter C. Nowell 教授以及賓夕法尼亞州個(gè)性化診斷中心主任合作���,開發(fā)一種能夠揭示胰腺癌患者何時(shí)患病的診斷測(cè)試�。
關(guān)于美迪西
美迪西(股票代碼:688202)成立于2004年��,總部位于上海���,致力于為全球制藥企業(yè)�����、研究機(jī)構(gòu)及科研工作者提供全方位的臨床前新藥研究服務(wù)���。美迪西的一站式綜合服務(wù)以強(qiáng)有力的項(xiàng)目管理和更高效、高性價(jià)比的研發(fā)服務(wù)助力客戶加速新藥研發(fā)進(jìn)程���,服務(wù)涵蓋醫(yī)藥臨床前新藥研究的全過程��,包括藥物發(fā)現(xiàn)�����、藥學(xué)研究及臨床前研究����。美迪西與國(guó)內(nèi)外優(yōu)質(zhì)客戶共同成長(zhǎng),為全球超過700家客戶提供新藥研發(fā)服務(wù)�,美迪西將繼續(xù)立足全球視野,聚力中國(guó)創(chuàng)新�����,為人類健康貢獻(xiàn)力量�!
聯(lián)系我們
Email:
marketing@medicilon.com.cn
電話: +86 (21) 5859-1500(總機(jī))










 相關(guān)新聞
相關(guān)新聞